«Адресная платформа химиотерапии»: российские учёные создали таргосомы для комплексного лечения и диагностики рака
Российские учёные разработали опытный препарат для диагностики и лечения онкологии на основе наночастиц из биосовместимого сополимера. Наночастицы адресно связываются с рецепторами раковых клеток и доставляют терапевтические препараты прямо в опухоль. Учёные поместили в частицы сразу три компонента: флуоресцентное вещество для диагностики опухоли, а также фотосенсибилизирующий и химиотерапевтический агенты. Препарат позволяет воздействовать на злокачественное образование сразу и химическими, и фотодинамическими методами. Эксперименты на животных показали высокую эффективность разработки, в будущем на её основе может быть создан препарат для лечения рака.

Одна из важных задач, над решением которой работают учёные всего мира, — создание таргетных методов диагностики и лечения рака. Традиционная химиотерапия имеет серьёзные побочные эффекты, поскольку препараты воздействуют не только на злокачественные, но и на здоровые ткани пациентов. Чтобы снизить негативные последствия терапии, ведётся поиск химических соединений, которые могут адресно взаимодействовать только с онкомаркерами — рецепторами на поверхности раковых клеток.
Как отметили авторы работы, наиболее перспективными платформами для создания адресных средств онкотерапии являются различные наноструктуры. В основе разработанного препарата — наночастицы из биосовместимого сополимера на основе молочной и гликолевой кислот (PLGA). Наночастицы из PLGA уже применяются в клинической практике за рубежом.
Для решения этой задачи биохимики совместили в новом препарате сразу две методики — классическую химиотерапию, но при этом целевого воздействия, а также фотодинамический подход. Фотодинамическая терапия применяется для лечения онкологии: в раковые ткани вводится фотосенсибилизирующее вещество, которое затем нагревается под воздействием лазера, это приводит к гибели клеток.
Авторы работы загрузили в полимерные наночастицы одновременно три агента: флуоресцентный краситель для диагностики опухолей, фотосенсибилизатор для фотодинамического воздействия и химиопрепарат. Биохимики также модифицировали поверхность наночастиц из PLGA таким образом, чтобы они нацеливались на особые белковые рецепторы HER2. Повышенная экспрессия (синтез) этих белков характерна для опухолей молочной железы, с HER2 учёные также связывают риски развития метастазов и низкой выживаемости пациентов. Полученные наноструктуры учёные назвали таргосомами.
Лабораторные исследования на животных доказали эффективность таргосом. Совместное действие различных активных компонентов даёт синергетический эффект и уничтожает более 90% раковых клеток.
«Именно комбинированное воздействие разными механизмами цитотоксичности — химиотерапевтическим препаратом иринотеканом и фотосенсибилизатором при подключении внешнего источника ИК-излучения — позволило достичь такой высокой терапевтической эффективности при лечении опухолей лабораторных грызунов», — рассказала RT заведующая лабораторией биохимических исследований канцерогенеза МФТИ Виктория Шипунова.
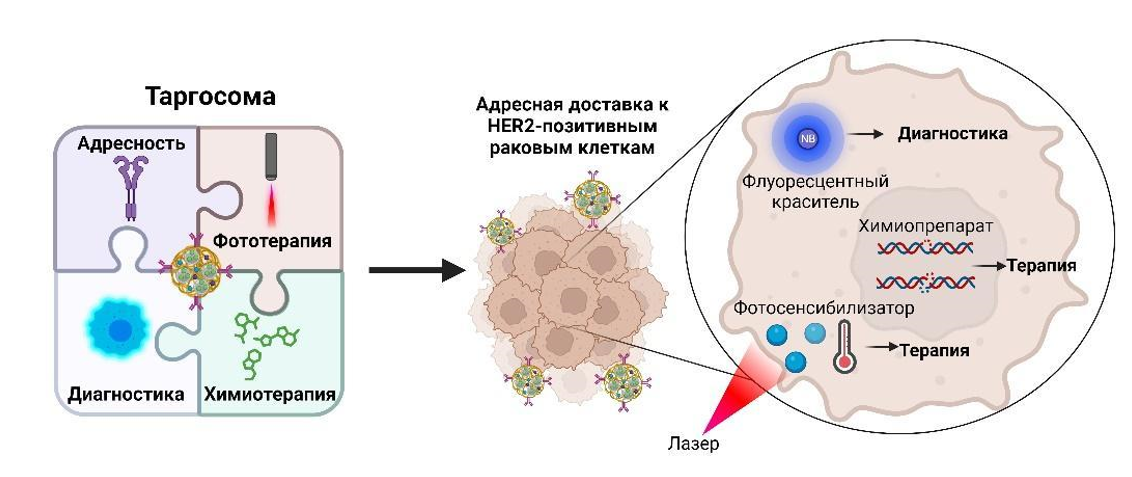
«Мультимодальные биосовместимые таргосомы являются препаратами медицины будущего, поскольку могут быть настроены на индивидуальные особенности каждого пациента. Это реальная основа для разработки лекарств персонализированной медицины. Уникальное сочетание в одной адресной платформе химиотерапии, диагностических и фототерапевтических свойств позволит достичь высокой эффективности в терапии и диагностике различных видов онкологических заболеваний», — пояснила RT аспирант лаборатории биохимических исследований канцерогенеза МФТИ Елена Комедчикова.

Gettyimages.ru © FatCamera
Учёные Института биофизики будущего МФТИ совместно с коллегами разработали новый экспериментальный препарат на основе наночастиц для прицельного уничтожения раковых клеток комбинацией фототерапии и таргетной химиотерапии. Лабораторные испытания на животных показали, что эффективность разработки превышает 90% — такой процент раковых клеток уничтожается в результате применения препарата. Об этом RT сообщили в пресс-службе Минобрнауки России. Исследование поддержано Минобрнауки и Российским научным фондом. Результаты опубликованы в Journal of Controlled Release.Одна из важных задач, над решением которой работают учёные всего мира, — создание таргетных методов диагностики и лечения рака. Традиционная химиотерапия имеет серьёзные побочные эффекты, поскольку препараты воздействуют не только на злокачественные, но и на здоровые ткани пациентов. Чтобы снизить негативные последствия терапии, ведётся поиск химических соединений, которые могут адресно взаимодействовать только с онкомаркерами — рецепторами на поверхности раковых клеток.
Как отметили авторы работы, наиболее перспективными платформами для создания адресных средств онкотерапии являются различные наноструктуры. В основе разработанного препарата — наночастицы из биосовместимого сополимера на основе молочной и гликолевой кислот (PLGA). Наночастицы из PLGA уже применяются в клинической практике за рубежом.

Gettyimages.ru © Evgenyi_Eg
В такие наночастицы могут быть загружены, как в контейнеры, различные соединения, поэтому они обладают огромным потенциалом в качестве переносчика для доставки препаратов непосредственно к клеткам-мишеням. Одной из серьёзных проблем при терапии рака является высокая приспособляемость опухоли к внешним воздействиям за счёт более быстрого деления и мутаций раковых клеток. Поэтому важно применять сразу целый комплекс методик, разрушающих опухоль, отмечают авторы исследования.Для решения этой задачи биохимики совместили в новом препарате сразу две методики — классическую химиотерапию, но при этом целевого воздействия, а также фотодинамический подход. Фотодинамическая терапия применяется для лечения онкологии: в раковые ткани вводится фотосенсибилизирующее вещество, которое затем нагревается под воздействием лазера, это приводит к гибели клеток.
Авторы работы загрузили в полимерные наночастицы одновременно три агента: флуоресцентный краситель для диагностики опухолей, фотосенсибилизатор для фотодинамического воздействия и химиопрепарат. Биохимики также модифицировали поверхность наночастиц из PLGA таким образом, чтобы они нацеливались на особые белковые рецепторы HER2. Повышенная экспрессия (синтез) этих белков характерна для опухолей молочной железы, с HER2 учёные также связывают риски развития метастазов и низкой выживаемости пациентов. Полученные наноструктуры учёные назвали таргосомами.
Лабораторные исследования на животных доказали эффективность таргосом. Совместное действие различных активных компонентов даёт синергетический эффект и уничтожает более 90% раковых клеток.
«Именно комбинированное воздействие разными механизмами цитотоксичности — химиотерапевтическим препаратом иринотеканом и фотосенсибилизатором при подключении внешнего источника ИК-излучения — позволило достичь такой высокой терапевтической эффективности при лечении опухолей лабораторных грызунов», — рассказала RT заведующая лабораторией биохимических исследований канцерогенеза МФТИ Виктория Шипунова.

© Journal of Controlled Release
Кроме того, препарат позволил визуализировать опухоль и метастазы. По словам учёных, разработка является отличным кандидатом на использование в медицинских препаратах.«Мультимодальные биосовместимые таргосомы являются препаратами медицины будущего, поскольку могут быть настроены на индивидуальные особенности каждого пациента. Это реальная основа для разработки лекарств персонализированной медицины. Уникальное сочетание в одной адресной платформе химиотерапии, диагностических и фототерапевтических свойств позволит достичь высокой эффективности в терапии и диагностике различных видов онкологических заболеваний», — пояснила RT аспирант лаборатории биохимических исследований канцерогенеза МФТИ Елена Комедчикова.
Читайте также
Альтернатива традиционным антибиотикам: учёные создали бактерицидный материал на основе наночастиц серебра
Наука и техника
Российские учёные совместно с коллегами из Бразилии разработали бактерицидный материал, который можно применять в составе красок и покрытий в инфекционных и хирургических отделениях. В перспективе разработка может также использоваться при создании медицинских имплантов. В её основе — глинистый материал с добавлением наночастиц серебра и фосфорномолибденовой кислоты. Последняя усиливает высвобождение ионов серебра, которые убивают патогенные микроорганизмы. Учёные из Губкинского университета,

Академик РАН Анаников: за фотокатализом будущее каталитических технологий
Наука и техника
Трем выдающимся российским ученым 12 декабря 2023 года вручили научную премию Сбера. О применении алгоритмов искусственного интеллекта (ИИ) для создания промышленных технологий нового поколения, важности научных грантов для проведения исследований и преимуществах фотокатализа в производстве препаратов ТАСС поговорил с одним из лауреатов премии, академиком Российской академии наук, заведующим лабораторией Института органической химии им. Н.Д. Зелинского РАН Валентином Ананиковым. — Расскажите о

Геометрия молекулы: российские учёные создали противораковые соединения на основе куркумина и фтора
Наука и техника
Российские учёные создали соединение на основе синтетического куркумина и фтора, которое обладает выраженным противоопухолевым эффектом. Такое вещество на 57% эффективнее подавляет рост раковых клеток в лабораторных условиях, чем куркумин в чистом виде. В новом исследовании специалисты определили, что атом фтора меняет геометрию молекулы куркумина и тем самым придаёт ей новые свойства. Именно это повышает противораковую активность соединения. Полученные результаты станут основой для дальнейших
Комментарии (0)
